هاله عدم رشد آنتی بیوتیک ها

مقدمه
فهرست
Toggleهاله عدم رشد آنتی بیوتیک یا “zone of inhibition” در آزمایش آنتی بیوگرام استفاده میشود تا مشخص شود یک آنتیبیوتیک خاص چقدر مؤثر است. این آزمایش معمولاً با استفاده از روش دیسک دیفیوژن (Kirby-Bauer) انجام میشود. در این روش، دیسکهای حاوی آنتیبیوتیکها روی سطح محیط کشت باکتریایی قرار میگیرند و پس از مدت زمانی، اندازه هالهای که در اطراف دیسک ایجاد میشود، اندازهگیری میشود.
اگر هاله عدم رشد بزرگتر باشد، نشاندهنده این است که آنتیبیوتیک اثر بیشتری بر روی آن باکتری دارد. در مقابل، یک هاله کوچک یا عدم وجود هاله به معنای مقاومت باکتری به آن آنتیبیوتیک است.
کنترل کیفیت آنتی بیوتیک ها
هدف از برنامه کنترل کیفیت، پایش و ارزیابی موارد زیر است:
- صحت و دقت روش انجام آزمایش تعیین حساسیت
- موارد و وسایل به کار برده شده در آزمایش
- عملکرد افرادی که آزمایش را انجام داده و نتایج به دست آمده را قرائت می نمایند.
به منظور دستیابی بهتر به این اهداف، در دسترس داشتن سویه های کنترل کیفیت تهیه شده از مراکز معتبر ضروری است.
ارگانیسم های مورد استفاده برای اهداف کنترل کیفیت می تواند از سویه های National Collection باشد. سویه های دیگری نیز ممکن است توسط سازنده محیط کشت به کار رود که شامل مجموعه ای از سویه های وحشی (Wild Strain) یا به دست آمده از نمونه های بیمار است که مختص هر آزمایشگاه بوده و برای انجام آزمایش های بیشتر به کار می روند.
برای انجام استاندارد کنترل کیفیت آنتی بیوتیک ها بهتر است از پلیت های 15 سانتی متر با روش شرح داده شده توسط CLSI
به عمق تقریبی 4 میلی متر معادل 60-70 میلی لیتر محیط و یا از پلیت های 10 سانتی متر تقریبا 25-30 میلی لیتر محیط استفاده شود.
دیسک ها را به گونه ای بر روی محیط قرار دهید که بین دو مرکز دیسک آنتی بیوتیک حداقل 24 میلی متر و از لبه صفحه بیشتر از 10-15 میلی متر فاصله داشته باشد. حداکثر 6 دیسک آنتی بیوتیک را می توان در یک پتری دیش 9 سانتی متری قرار دارد. اگر مناطق بازدارنده همپوشانی پیدا کرد، باید تعداد دیسک ها را در هر صفحه کاهش یابد.
ظرف 15 دقیقه پس از تنظیم کدورت، یک سواب پنبه ای استریل را در سوسپانسیون باکتریایی استاندارد فرو کنید و بر روی محیط کشت دهید.

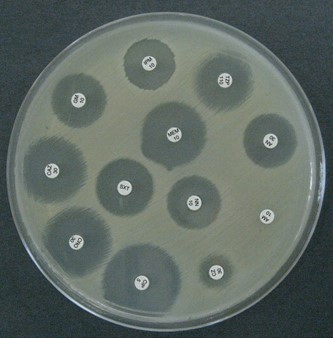
معیار های رد نتایج:
پلیت هایی را که دارای کلنی های جدا شده یا با رشد کمتر از یکنواخت هستند، مردود است.
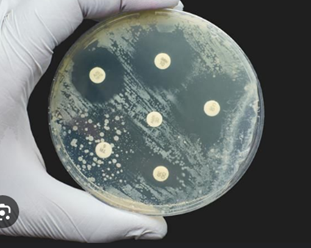
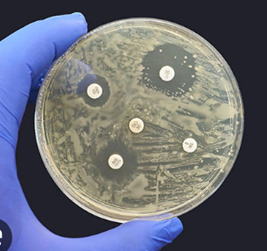
هاله های عدم رشد را که در آن دو دیسک با هم همپوشانی دارند، مردود است.
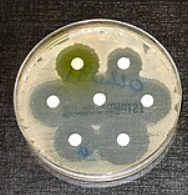
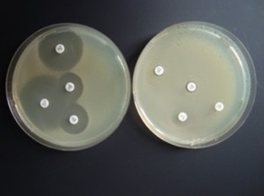
هاله های عدم رشد را که دایره ای نیستند یا دارای جداره دندانه دار هستند، مردود است.

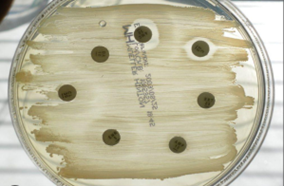
سویه های روتین کنترل کیفیت پیشنهادی توسط CLSI عبارتند از:
Enterococcus faecalis ATCC 29212
Escherichia coli ATCC 25922
Pseudomonas aeruginosa ATCC 27853
Staphylococcus aureus ATCC 25923
E.faecalis ATCC 33186
برای ارزیابی محیط مولر هینتون آگار از دیسک تری متوپریم سولفامتوکسازول استفاده می شود. در محیط کشت قابل قبول، هاله عدم رشد به قطر 29 میلی متر یا بزرگ تر ایجاد می شود. در حالی که در محیط های کشت غیر قابل قبول، هاله عدم رشد ایجاد نمی شود یا در داخل هاله، رشد کم مشاهده می شود و یا هاله ای با قطر کمتر از 20 میل متر ایجاد می گردد. این آزمون به منظور بررسی مقادیر غیرقابل قبول تیمیدین در محیط کشت مزبور است. هم چنین Entrococcus faecalis ATCC 29212 برای کنترل دیسک های آمینوگلیوکوزید با دوز بالا به کار می رود.
E.coli ATCC 35218 فقط به عنوان یک میکروارگانیسم کنترلی برای ترکیبات ممانعت کننده بتالاکتاماز، مثل ترکیبات حاوی کلاولانیک اسید، سولباکتام یا تازوباکتام پیشنهاد می شود.
Klebsiella pneumoniae ATCC 700603 به عنوان یک سویه کنترلی برای آزمایش های ESBL به کار برده می شود.
گروه بندی آنتی بیوتیک ها از نظر کاربرد بالینی:
گروه A – جهت آزمایش و گزارش روتین نتایج گروه های خاص باکتریایی در نظر گرفته می شود.
گروه B – داروهای مورد مصرف برای آزمایش های اولیه است و زمانی که نتایج به صورت انتخابی گزارش می گردد مانند:
- سفالوسپورین های نسل سوم برای باسیل های روده ای جدا شده از CSF
- تری متوپریم سولفامتوکسازول برای باکتری های جدا شده از ادرار
- عفونت های چند میکروبی
- عفونت در کانون های مختلف
- وجود آلرژی به داروهای اولیه
- عدم تحمل و یا عدم پاسخ به داروهای گروه A
- برای اهداف کنترل عفونت
گروه C – معرف داروهای جایگزین یا اضافی است که در موارد زیر به کار می شود.
- وجود سویه های مقاوم به چند دارو
- در بیماران با آلرژی به داروهای اولیه
- درمان باکتری های غیرمتعارف
- کنترل عفونت
گروه U- عوامل ضدمیکروبی که در مرحله اول صرفا برای درمان عفونت های ادراری مصرف می شوند. این داروها نباید برای پاتوژن های جدا شده از سایر نواحی به صورت روتین استفاده می شود.
گروه O- عوامل ضدمیکروبی هستند که کاربرد بالینی برای باکتری دارد، اما برای آزمایش روتین داروی انتخابی نیست.
گروه Inv- عوامل ضدمیکروبی است که برای گروهی از ارگانیسم ها جنبه تحقیقاتی دارد و هنوز تایید نشده است.
استاندارد کنترل کیفیت دیسکهای آنتیبیوتیکی CLSI M100 (2024)
| نتیجه گیری پس از تکرار تست | تعداد خارج از محدوده پس از آزمایش تکراری ( بر اساس هر 30 تکرار) | نتیجه گیری برای ارزیابی اولیه با 15 تکرار (3 تکرار در 5 روز) | تعداد نتیجه خارج از محدوده برای ارزیابی اولیه با 15 تکرار (3 تکرار در 5 روز) |
| لازم نیست | لازم نیست | نتیجه موفقیت آمیز است تبدیل به کنترل هفتگی کنید | 0-1 |
| آزمایش قابل قبول است و کنترل کیفیت را به هفتگی تغییر دهید. | 2-3 | 3 تکرار در 5 روز را مجددا آزمایش کنید | 2-3 |
| نتیجه شکست خورده است بررسی کنید و در صورت لزوم اقدام اصلاحی انجام دهید. و کنترل کیفیت را روزانه انجام دهید. | بیشتر از 4 | نتیجه شکست خورده است بررسی کنید و در صورت لزوم اقدام اصلاحی انجام دهید و کنترل کیفیت را روزانه انجام دهید. | بیشتر از 4 |
کنترل کیفیت اولیه برای آنتی بیوتیک جدید
در صورت استفاده از یک دیسک آنتی بیوتیک جدید که قبلا آن آنتی بیوتیک در آزمایشگاه استفاده نشده است ، آزمایشگاهها باید 15 مرتبه ( مثلا در 5 روز کاری ، هر روز سه بار ) و یا طی 20تا 30روز کاری متوالی کنترل کیفیت را انجام دهند.
کنترل کیفیت پس از تغییر برند یا لات نامبر
در صورت تغییر تولیدکننده ، برند دیسک یا لات نامبر دیسک، کنترل کیفیت به مدت 1 روز انجام میشود.این گام به آزمایشگاهها کمک میکند تا از سازگاری و کیفیت دیسکها در شرایط عملی اطمینان حاصل کنند.
کنترل کیفیت هفتگی
پس از گذراندن دوره اولیه کنترل کیفیت ، اگر نتایج دیسکها پایدار باشند، کنترل کیفیت به صورت هفتگی ادامه مییابد. و در صورت تغییر لات فقط یکبار کنترل کیفیت در ابتدای کار کفایت میکند تا صحت عملکرد دیسک ها تایید شود این رویه تضمین میکند که آزمایشگاهها بهصورت مستمر از صحت عملکرد دیسکها اطمینان داشته باشند.
نتایج خارج از محدوده کنترل کیفیت و اقدامات اصلاحی
اگر هر یک از نتایج کنترل کیفیت هفتگی خارج از محدوده قابل قبول باشد، انجام اقدامات اصلاحی مورد نیاز است. نتایج خارج از محدوده کنترل را میتوان به خطای تصادفی، خطای قابل شناسایی یا خطای مربوط به سیستم طبقه بندی کرد. نتایج خارج از محدوده با سویه های کنترل به دلیل خطاهای تصادفی یا قابل شناسایی معمولا با یک بار تکرار آزمایش قابل حل هستند. نتایج خارج از محدوده اغلب نتیجه آلودگی یا استفاده از سویه نادرست است. اقدام اصلاحی ابتدا باید شامل تکرار آزمایش با کشت خالص یک سویه تازه کشت شده باشد. نتایج خارج از محدوده که به دلیل خطای سیستماتیک معمولا با تکرار آزمایش اصلاح نمی شوند و ممکن است نشان دهنده یک مشکل جدی باشد که میتواند بر نتایج بیمار تاثیر منفی بگذارد. هر نتیجه خارج از محدوده باید بررسی شود.
اقدامات اصلاحی زمانی که هاله عدم رشد به دلیل خطاهای مشهود و واضح زیر خارج از محدوده مجاز قرار گرفته باشد:
- استفاده از دیسک اشتباه
- استفاده از سویه کنترلی اشتباه
- آلودگی واضح سویه
- استفاده غیرعمدی از دما و شرایط انکوباسیون اشتباه
در این حال باید دلیل ایجاد خطا مکتوب و پس از اصلاح آزمایش دوباره تکرار شود. اگر نتایج گزارش شده در محدوده مورد نظر قرار گرفت، عملیات اصلاحی بیشتری مورد نیاز نمی باشد.
اقدامات اصلاحی زمانی که هاله عدم رشد به دلیل خطاهای نامشخص خارج از محدوده مجاز قرار گرفته باشد:
آزمایش را جهت یک سویه کنترلی یا دیسک آنتی بیوتیک برای 5 روز متوالی تکرار و همه نتایج را ثبت کنید.
اگر اندازه قطر هاله در همه 5 روز متوالی در محدوده مجاز باشد، عملیات اصلاحی بیشتری مورد نیاز نیست.
اگر اندازه قطر هاله در همه 5 روز متوالی خارج از محدوده مجاز باشد، به عملیات اصلاحی اضافی نیاز نیست. و باید آزمایش های کنترلی روزانه ادامه داده شود تا به دلیل نهایی مشکل پی برده شود.
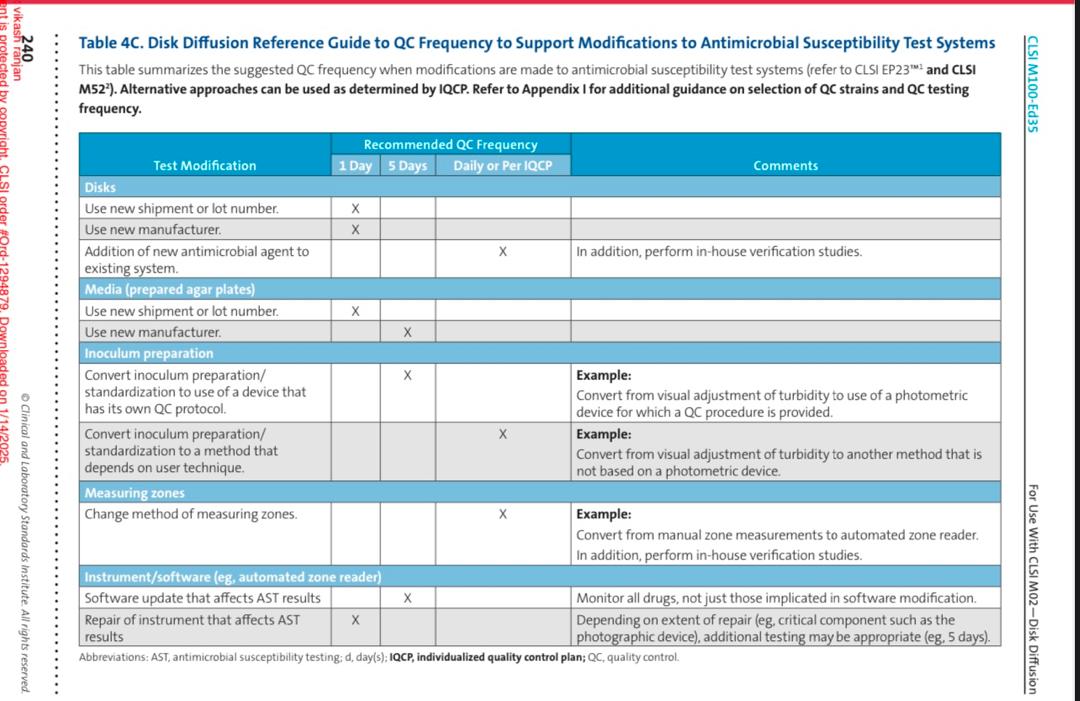
جدول تغییرات نسخه ی2025 CLSI- M100
کتاب کنترل کیفیت در بخش میکروب شناسی و بخش های کیفی (جلد 6) – دکتر جباری
پیوست
پوستر تریتا جدول هاله عدم رشد آنتی بیوتیک ها 2024
پوستر تریتا جدول هاله عدم رشد آنتی بیوتیک ها 2025
جدول هاله عدم رشد آنتی بیوتیک CLSI-M100 Ed34 2024
استاندارد عملكردي آزمايش تعيين حساسيت ضدميكروبي به روش انتشار از دیسک CLSI Farsi S21
کتاب آنتی بیوتیک مرجع WHO Antibiotic Book






دیدگاهتان را بنویسید